
[教育和科研经历]
刘光慧(1979.4.8—),中国科学院生物物理研究所研究员,中国科学院特聘研究员。国家杰出青年科学基金获得者,干细胞国家重大科学研究计划(973)项目首席科学家。出生于辽宁省辽阳市。近年来在人类衰老、基因编辑和再生医学领域取得系列原创性研究成果,以通讯作者在Nature,Science,Cell,Cell Stem Cell, Nature Communications和Cell Res等刊物发表系列研究论文,授权或申请发明专利16项。多次应邀在国际学术会议做大会报告,并应邀同美国科学院、俄罗斯科学院、加拿大衰老研究学会、德国洪堡基金会、日本领军人才计划(作为Future Leader 2017)等专家进行学术交流。获“首届老年医学杰出贡献奖”,“树兰医学青年奖”,“中国科学院青年科学家奖”,“中国细胞生物学会青年研究员奖”,“贝时璋青年生物物理学家奖”,“大挑战青年科学家奖”。
[主要学术贡献]
刘光慧的工作紧扣“利用干细胞和基因编辑技术研究和治疗衰老相关疾病”展开。(1)在衰老和疾病机制研究方面:相继建立儿童早衰症、成年早衰症、帕金森病、渐冻人、范可尼贫血症、镰刀形细胞贫血症、着色性干皮病等人类干细胞疾病模型,揭示细胞核结构和表观遗传改变是多种衰老相关疾病的共性分子基础有关机制;(2)在基于干细胞的基因治疗方面:突破技术瓶颈,首次在病人iPSC中利用HDAdV技术实现基因突变的高效靶向矫正,并率先证明基因矫正工具的安全性,发展安全高效基因矫正载体telHDAdV,并已成功修复8 种致病基因突变。(3)首次揭示异染色质结构失序是人类干细胞衰老的驱动力。(4)发展染色质三维动态成像工具TTALE,揭示核仁区核糖体DNA重复序列的减损是新型人类衰老标记物。(5)利用基因编辑获得了第一例人类遗传增强干细胞。(6)发现一系列延缓干细胞衰老或干预衰老相关疾病的候选化合物。刘光慧现任中国生物物理学会衰老生物学分会副理事长,中国老年学和老年医学学会抗衰老分会副主任委员,老年医学学会基础与转化医学分会副会长,中国老年医学研究机构联盟副主任委员,中国抗衰老促进会再生医学专业委员会副主任委员,中国细胞生物学会再生细胞生物学分会副会长,Protein & Cell杂志副主编。获“首届老年医学杰出贡献奖”,“树兰医学青年奖”,“中国科学院青年科学家奖”,“中国细胞生物学会青年研究员奖”,“贝时璋青年生物物理学家奖”,“大挑战青年科学家奖”。
[心路历程]
感谢树兰医学评审委员会授予我2017年树兰医学青年奖,这不仅是我个人的荣誉,更是我们研究团队以及所有合作者的共同荣誉,是对我们近年来科研工作的肯定。
目前,中国乃至全球都正面临人口老龄化的严峻考验。衰老是人类最大的致病因子,与阿尔兹海默症、骨质疏松、糖尿病和肿瘤等多种退行性疾病密切相关,严重影响人口健康和生活质量。同时,历经岁月的洗礼,仍能老而不衰,保持健康的体魄和充沛的精力又是每个人心驰神往的境界,因此,深入探究衰老机理并着眼于衰老主动预防,避免机体未老先衰,延长机体健康寿命,是亟待解决的社会问题,更是现代生命科学的重要使命,而这也正是我们研究团队聚焦的核心问题。
人体内存在一群充满活力的“种子”细胞---成体干细胞,它们不仅能自我更新,还能在特定条件下分化成心肌细胞、神经细胞和造血细胞等功能性体细胞,因此被认为是维持机体正常更新,或者进行创伤后修复的重要源泉。衰老是机体各组织器官功能随增龄而发生退行性变化的过程。干细胞衰老学说认为,在机体衰老过程中,成体干细胞的衰老乃至耗竭是组织器官衰老和老年性疾病的重要诱因。因此,要研究涉及不同组织器官的机体衰老,就需要发现神经干细胞、造血干细胞和间充质干细胞等不同成体干细胞发生衰老的分子细胞机制,进而揭示机体衰老和衰老相关疾病发生和发展的规律,从而为干预衰老相关通路、维持成体干细胞“年轻态”,乃至延缓机体衰老和实现健康老龄化提供有力的科学依据。
人类的衰老受到遗传基因、生活环境、个人习惯以及饮食爱好等方方面面的影响。科学家们最初选择使用酵母、线虫、果蝇或小鼠等相对简单的模式生物来研究衰老。然而,长期的研究结果表明,通过这些模式生物获得的衰老机制或干预手段并不能完全应用到人类的衰老研究中。因此,我们研究团队一直致力于通过建立人类干细胞衰老模型来开展衰老相关的基础和转化医学研究。2012年,我受到中组部青年千人计划的资助,回到中国科学院生物物理研究所组建了衰老与再生课题组。经过5年的不懈努力,我们研究团队基于人多能干细胞和基因编辑技术建立了成熟稳定的人类干细胞衰老研究体系,发展了一系列新型研究策略和方法,通过在人多能干细胞中编辑与衰老、寿命或衰老相关疾病密切相关的一系列重要基因,在实验室中模拟了人类成体干细胞的衰老以及由衰老引起的多种组织器官病变表型,进而通过多层次的机制研究提出了新型人类衰老研究理论和创新性的研究思路。
这里列举我们团队的两个研究:
(1)发现遗传物质包装方式的改变是衰老的重要驱动力之一。成年早衰症是一种罕见疾病。患者表现出全身多器官多系统的加速衰老,在20-30岁时就会罹患白内障,并多发骨质疏松、二型糖尿病、心脏病和肿瘤等典型的衰老相关疾病。尽管人们已经了解成年早衰症是由于负责DNA损伤修复的WRN蛋白的缺失所致,但是这个“早衰症蛋白”的缺失引发机体衰老的分子和细胞机制却始终是一个未解之谜。基于研究团队建立的干细胞衰老研究平台,我们首先利用“基因剪刀”在人多能干细胞中精准删除了这个早衰症蛋白,发现细胞很快表现出了“衰老的症状”。接下来,利用表观遗传组学测序等多种先进的现代生物学技术,我们发现这种过早过快地衰老与细胞内的遗传物质如何被“包装”密切相关。人类的基因并不是无序的漂浮在细胞中,遗传物质在细胞核中必须和相关蛋白质相互缠绕形成复杂的高级结构才能发挥正常的功能。我们发现“早衰症蛋白”的缺失会导致遗传物质的包装变得更加凌乱和松散,而这种遗传物质高级结构的失序又会进一步诱发细胞衰老。我们的这项研究为干预人类细胞衰老提供了重要线索,即保持或恢复细胞中遗传物质的正确包装有可能延缓甚至逆转细胞的衰老,进而促进人类的健康长寿。美国国家衰老研究院Robert Brosh教授也对我们的研究进行了中肯的评价,认为这项工作确立了人类遗传物质包装形式的改变在驱动细胞衰老中发挥的核心作用。
(2)通过编辑基因组DNA的单个核苷酸获得了既可以延缓细胞衰老又能够抵抗肿瘤发生的“遗传增强”干细胞。近年来,围绕干细胞技术的再生医学领域蓬勃发展。然而,该领域的研究人员面临着两大难题:一是干细胞植入体内后,会随着细胞分裂而逐步“变老”,丧失干细胞潜能;二是有些干细胞会变得非常“疯狂”,这些细胞增殖异常旺盛,最终发展成肿瘤,从而带来极大的安全隐患。长期以来,这两大难题制约着干细胞治疗的发展。我们研究团队发现,只要靶向编辑某特定基因的单个碱基,即可达到延缓衰老和抵抗肿瘤这两个方面的平衡。其实,这个发现始于对延缓衰老基因与药物的筛选。我们发现很多成功延缓衰老的策略都与一个抗氧化转录因子NRF2的激活密不可分,因此我们大胆提出假设,如果通过在基因层面进行编辑,使NRF2内源性激活,是否可以使人类干细胞抵抗衰老呢?基于这一设想,我们首先通过“基因剪刀”在人类基因组水平增强了NRF2活性,使其更加稳定,并持续调动其下游靶基因,使得这些下游靶基因可以不断的发挥抵御外界不利环境和清除细胞内活性氧等有害分子的作用。当把这类遗传增强干细胞注入到小鼠后肢的缺血部位,可以帮助小鼠后肢迅速重建血管系统,从而展现出很好的治疗能力。另一方面,将其移植入免疫缺陷小鼠体内后,发现这类细胞并不会形成肿瘤,甚至在强致癌条件下该细胞也具有极强的抑制成瘤能力。由此可见,通过简单的单核苷酸改变,就可以产生一种既抵抗细胞衰老,又能够抑制肿瘤生成的“遗传增强干细胞”,成功印证了“四两拨千斤”的道理。更为重要的是,这项研究使未来规模化和标准化制备优质安全的人类干细胞移植材料成为可能。
干细胞和基因编辑,这两项在21世纪突飞猛进的重要生物学技术的双剑合璧,使我们能够快速稳定地建立多种罕见早衰症以及其它不同种类衰老相关疾病的细胞模型,从而推动了相关的衰老机制研究、药物筛选和干细胞治疗等基础及转化研究的快速发展,未来还将进一步帮助我们回答“我们为什么衰老”,“我们到底有多老”,以及“我们是否能够健康衰老”等重要科学问题。延年益寿,关乎每个人的生存质量和幸福指数,也是人类追寻了几千年的梦想。我和我们的研究团队将继续砥砺前行,不断创新,力争为衰老生物学和老年医学的发展贡献更大的力量。
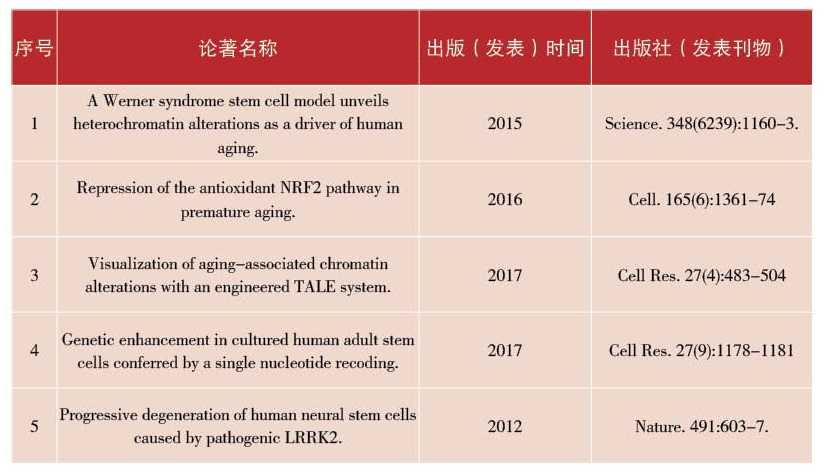
[代表性著作]
[获奖者风采]

[提名人]
